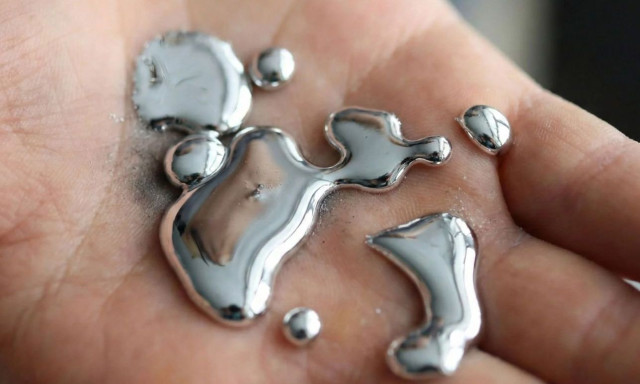
Αυτό το μέταλλο λιώνει στα χέρια σου – Και οι επιστήμονες μόλις ανακάλυψαν κάτι παράξενο
Ένα μέταλλο που δεν ακολουθεί τους κανόνες
Snapshot
- Το γάλλιο λιώνει θερμοκρασία περίπου 30°C και παρουσιάζει ασυνήθιστη συμπεριφορά που ανατρέπει παλιές θεωρίες για τη δομή του υγρού μετάλλου.
- Νέα έρευνα δείχνει ότι οι ομοιοπολικοί δεσμοί που υπάρχουν στο στερεό γάλλιο εξαφανίζονται κατά την τήξη και επανεμφανίζονται σε υψηλότερες θερμοκρασίες.
- Η ηλεκτρική αγωγιμότητα του γαλλίου βελτιώνεται με την τήξη και μειώνεται μη γραμμικά με περαιτέρω αύξηση της θερμοκρασίας, συνδεόμενη με τη δομική οργάνωση του υγρού.
- Η επιφάνεια του υγρού γαλλίου παρουσιάζει μια λεπτή αλλά μετρήσιμη γεωμετρική οργάνωση σε ατομικό επίπεδο, παρά την αναμενόμενη αταξία των υγρών.
- Η κατανόηση της συμπεριφοράς του γαλλίου ενισχύει τις δυνατότητες σχεδιασμού υγρών μετάλλων με ελεγχόμενες ιδιότητες για εφαρμογές σε τεχνολογίες επόμενης γενιάς.
Ένα μέταλλο που μπορεί να λιώσει μέσα στην παλάμη σου συνεχίζει να εκπλήσσει την επιστημονική κοινότητα, φέρνοντας τα πάνω κάτω σε θεωρίες δεκαετιών.
Το γάλλιο, που ανακαλύφθηκε το 1875, είναι ήδη γνωστό για την αλλόκοτη συμπεριφορά του. Λιώνει περίπου στους 30 βαθμούς Κελσίου, γεγονός που σημαίνει ότι μπορεί να μετατραπεί σε υγρό ακόμη και σε ένα ζεστό δωμάτιο ή μέσα σε ένα φλιτζάνι τσάι. Παρά τη σημαντική του χρήση σε ημιαγωγούς, LED και φωτοβολταϊκά συστήματα, η υγρή του μορφή παρέμενε μέχρι σήμερα σε μεγάλο βαθμό ένα «μυστήριο».
Τώρα, επιστήμονες από το Πανεπιστήμιο του Όκλαντ υποστηρίζουν ότι έλυσαν έναν γρίφο που απασχολούσε την έρευνα για περισσότερα από 30 χρόνια, ανατρέποντας μια βασική παραδοχή για τη δομή του υγρού γαλλίου.
Ένα μέταλλο που δεν ακολουθεί τους κανόνες
Σε ατομικό επίπεδο, το γάλλιο δεν συμπεριφέρεται όπως τα περισσότερα μέταλλα. Στη στερεά του μορφή, τα άτομα σχηματίζουν ζεύγη (διμερή) και συνδέονται με ομοιοπολικούς δεσμούς, μοιράζοντας ηλεκτρόνια – μια συμπεριφορά που θυμίζει περισσότερο αμέταλλα.
Ακόμη πιο παράξενο είναι ότι το στερεό γάλλιο είναι λιγότερο πυκνό από το υγρό του, όπως ακριβώς συμβαίνει με τον πάγο που επιπλέει στο νερό.
Για χρόνια, οι επιστήμονες πίστευαν ότι αυτοί οι ομοιοπολικοί δεσμοί επιβιώνουν και στη υγρή φάση, εξηγώντας τις ιδιαιτερότητές του.
Η νέα μελέτη, όμως, δείχνει το αντίθετο.
Με τη βοήθεια προσομοιώσεων μεγάλης κλίμακας που καταγράφουν με ακρίβεια την κίνηση των ατόμων, οι ερευνητές διαπίστωσαν ότι οι δεσμοί αυτοί εξαφανίζονται ακριβώς τη στιγμή της τήξης. Το εντυπωσιακό είναι πως επανεμφανίζονται όταν η θερμοκρασία αυξάνεται ακόμη περισσότερο.
Το «παράδοξο» της ηλεκτρικής αγωγιμότητας
Η ανατροπή αυτή βοηθά να εξηγηθεί και ένα παλιό επιστημονικό αίνιγμα. Όταν το γάλλιο λιώνει, η ηλεκτρική του αγωγιμότητα βελτιώνεται, καθώς η αντίστασή του μειώνεται. Ωστόσο, όσο το υγρό θερμαίνεται περαιτέρω, η αντίσταση αυξάνεται ξανά με μη γραμμικό τρόπο.
Οι ερευνητές συνδέουν αυτή τη συμπεριφορά με την επανεμφάνιση της δομικής οργάνωσης σε υψηλότερες θερμοκρασίες.
Κεντρικό ρόλο φαίνεται να παίζει η εντροπία, δηλαδή το μέτρο της αταξίας. Κατά την τήξη, όταν οι δεσμοί σπάνε, η αταξία αυξάνεται απότομα, γεγονός που σταθεροποιεί το υγρό και μειώνει το σημείο τήξης.
«Τριάντα χρόνια επιστημονικής βιβλιογραφίας βασίζονταν σε μια θεμελιώδη παραδοχή που τελικά δεν ισχύει», σημειώνει η καθηγήτρια Νίκολα Γκάστον από το Πανεπιστήμιο του Όκλαντ και το Ινστιτούτο MacDiarmid.
Γιατί το γάλλιο έχει τόσο μεγάλη σημασία
Το γάλλιο βρίσκεται στο επίκεντρο μιας ανερχόμενης κατηγορίας υλικών, των λεγόμενων «υγρών μετάλλων», τα οποία θεωρούνται πολλά υποσχόμενα για τεχνολογίες επόμενης γενιάς.
Χάρη στη χαμηλή θερμοκρασία τήξης του, μπορεί να διαλύει άλλα μέταλλα και να σχηματίζει κράματα που χρησιμοποιούνται στην κατάλυση, στα ενεργειακά συστήματα και στην προηγμένη κατασκευή. Ορισμένα από αυτά τα υλικά έχουν μάλιστα την ικανότητα να αυτοοργανώνονται, δημιουργώντας δομές με χρήσιμες ιδιότητες.
Η καλύτερη κατανόηση της συμπεριφοράς του γαλλίου σε διαφορετικές θερμοκρασίες θα μπορούσε να επιτρέψει τον σχεδιασμό υγρών μετάλλων με ακριβώς ελεγχόμενες ηλεκτρικές, θερμικές και χημικές ιδιότητες, με εφαρμογές σε μπαταρίες, εύκαμπτα ηλεκτρονικά και αποδοτικούς καταλύτες.
Η σημαντική αυτή πρόοδος προέκυψε όταν η δρ Στεφ Λάμπι επανεξέτασε δεκαετίες πειραματικών δεδομένων και τα συνέκρινε με σύγχρονες προσομοιώσεις, γεφυρώνοντας αντικρουόμενα αποτελέσματα. Η μελέτη δημοσιεύθηκε στο περιοδικό Materials Horizons.
Κρυφή τάξη στην επιφάνεια ενός υγρού
Σε δεύτερη μελέτη, η ίδια ερευνητική ομάδα εστίασε σε ένα ακόμη παλιό ερώτημα: είναι πράγματι εντελώς άτακτη η επιφάνεια του υγρού γαλλίου;
Παρότι τα υγρά χαρακτηρίζονται από συνεχή κίνηση και αταξία, τα ευρήματα δείχνουν ότι η επιφάνεια του γαλλίου παρουσιάζει μια λεπτή αλλά μετρήσιμη γεωμετρική οργάνωση.
Συγκεκριμένα, η δομή αυτή εκτείνεται σε περίπου τρία ατομικά στρώματα και δεν μεταβαίνει πλήρως σε «χαοτική» κατάσταση παρά μόνο σε απόσταση περίπου 8,5 ångström από την επιφάνεια.
Μέσα σε αυτά τα στρώματα, τα άτομα σχηματίζουν δύο διακριτά «κελύφη» γύρω από ένα κεντρικό άτομο, σε αποστάσεις περίπου 3 και 5,4 ångström, δημιουργώντας μοτίβα με συγκεκριμένη γωνιακή συμμετρία.
Η μελέτη έδειξε επίσης ότι ένα λεπτό στρώμα οξειδίου ενισχύει αυτή την τάξη, καθιστώντας τη δομή πιο συμπαγή. Αντίθετα, η προσθήκη ενός μόνο ατόμου βισμουθίου αρκεί για να διαταράξει το μοτίβο, επαναφέροντας μια πιο χαοτική δομή.
Το παράδοξο της «τάξης μέσα στην αταξία»
Τα αποτελέσματα αυτά αποκαλύπτουν ότι ακόμη και σε υγρή κατάσταση, το γάλλιο μπορεί να εμφανίζει κρυφά επίπεδα οργάνωσης.
Η κατανόηση και ο έλεγχος αυτής της συμπεριφοράς ενδέχεται να αποδειχθούν κρίσιμα για την εξέλιξη των τεχνολογιών υγρών μετάλλων, όπου οι ιδιότητες της επιφάνειας συχνά καθορίζουν την απόδοση.
Για ένα υλικό που λιώνει στο χέρι, το γάλλιο αποδεικνύεται πολύ πιο πολύπλοκο απ’ όσο φαινόταν, δείχνοντας ότι ακόμη και μέσα στην αταξία μπορεί να κρύβεται μια απρόσμενη τάξη.